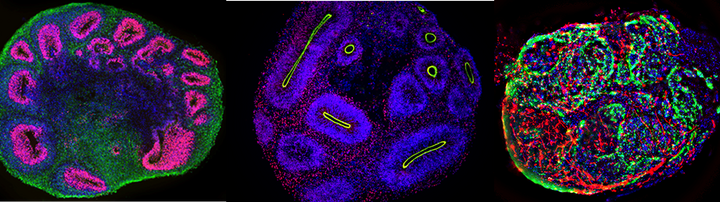
Organoids
Agnieszka Rybak-Wolf
Profil
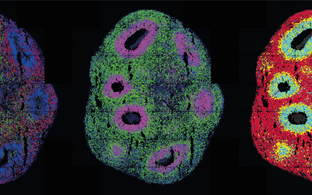
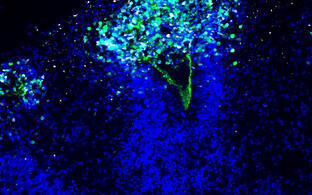
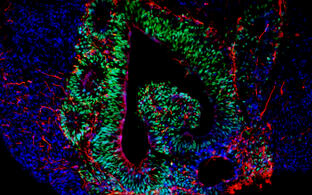
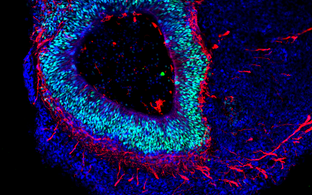
Die Organe des menschlichen Körpers bestehen aus verschiedenen Zelltypen, die so organisiert sind, dass sie ein mehrschichtiges Netzwerk bilden. Heute ist es möglich, organartiges Gewebe (Organoide) im Labor zu rekonstruieren. Stammzellen werden dabei durch molekulare Signale dazu gebracht, sich zu differenzieren und in Kultursystemen gezüchtet, die ihre dreidimensionale Selbstorganisation fördern. Die sich rasch entwickelnde Organoid-Technologie ermöglicht es, die Zellstruktur phänotypisch zu kopieren. Bis zu einem gewissen Grad gilt das auch für die Funktionen verschiedener menschlicher Organe (beispielsweise Gehirn, Schilddrüse, Thymus, Darm, Leber, Bauchspeicheldrüse, Magen, Lunge, Niere) und sogar für Embryos im Frühstadium.
Als beinahe-physiologische 3D-Kultursysteme eröffnen Organoide uns neue Möglichkeiten, die Entwicklung gesunder und erkrankter Organe zu untersuchen und bieten großes Potenzial für die translationale Forschung.
Unsere Werkzeuge
- Gen-Editierung, Einführung/Korrektur krankhafter Mutation
- Herstellung von Gehirn-Organoiden
- Organoid-Charakterisierung durch Standardtechniken der Molekularbiologie:
NanoString genomische Analyse, qPCR und Immunhistochemie, Mikroelektroden-Arrays (MEAs) - in vitro-Krankheitsmodellierung
- RNAseq und Einzelzell-Sequenzierung
Technologie
Kultursysteme für Gehirn-Organoide
Die 2019 etablierte Organoid-Plattform unterstützt die Forschung, die mit Organoiden arbeitet, indem sie Expertise zur Organoidherstellung aus pluripotenten Stamm- oder Vorläuferzellen zu Verfügung stellt und Methoden für ihre Charakterisierung entwickelt. Die Plattform gehört zum Berliner Institut für Medizinische Systembiologie (BIMSB) am Max-Delbrück-Centrum. Zurzeit liegt unser Schwerpunkt auf verschiedenen Arten von Gehirn-Organoiden. Doch das Angebot an vereinfachten Mini-Organen wird sich mit der Weiterentwicklung der Plattform vergrößern.
Ein Hauptziel unserer Plattform besteht darin, Kultursysteme für Gehirn-Organoide weiterzuentwickeln und die in vitro-Morphogenese neuralen Gewebes zu verbessern. Wir möchten Technologie etablieren, die Gehirn-Organoide vaskularisiert und Mikroglia (ein nicht-neuronaler Zelltyp im Zentralnervensystem) in unsere Systeme integriert, um die langfristige Reifung dreidimensionaler neuraler Gewebe zu erreichen.
Außerdem etablieren wir Methoden, zu denen bereits publiziert wurde und entwickeln neue Herangehensweisen in der Organoidforschung. Ein besonderer Schwerpunkt liegt auf Technologien wie der Einzelzell-Sequenzierung, dem RNA targeting sowie Bearbeitung des Erbguts mit CRISPR-Cas-Systemen.
Krankheitsmechanismen gemeinsam analysieren
In enger Zusammenarbeit mit der Plattform für pluripotente Stammzellen und der Transgenics-Plattform am Max-Delbrück-Centrum werden wir Techniken der Genom-Editierung anwenden, um genetisch bedingte Krankheiten des Gehirns zu modellieren und zu erforschen. Das Leigh-Syndrom (eine erbliche psychomotorische Rückbildung im Kleinkindalter) und Alzheimer gehören zu den Beispielen, an denen wir die grundlegenden molekularen Mechanismen analysieren und bei denen wir mögliche Wirkstoffe screenen.
Unser langfristiges Ziel ist es, eine umfassende Blaupause für moderne Gentherapien bei genetisch bedingten Krankheiten des Gehirns zu erarbeiten. Dafür möchten wir personalisierte, aus Patient*innenzellen gezüchtete Gehirn-Organoid-Modelle mit den neuesten Werkzeugen zur Genreparatur kombinieren.